МИКРОЭЛЕМЕНТЫ В ПРИРОДЕ
Известно, что для нормального роста и развития растениям необходимы вода, воздух, свет, тепло и питательные вещества. Эти факторы играют важнейшую роль в жизни растений.
Азот, фосфор, калий, кальций, магний, железо содержатся в растениях в относительно больших количествах. Их называют макроэлементами.
Бор, марганец, медь, цинк, кобальт, молибден и некоторые другие элементы находятся в растениях в незначительных количествах и называются микроэлементами (табл. 1).
|
Таблица 1 Среднее содержание основных макро- и микроэлементов в растениях
|
Всего лишь 50 лет назад считалось, что около десяти элементов, составляющих основную массу живого вещества (—99,4%) таких, как углерод, кислород, водород, азот, фосфор, калий, кальций, магний, железо и сера, вполне достаточно для нормального роста растений. В настоящее время учеными доказано, что без микроэлементов невозможна нормальная жизнедеятельность растительных и животных организмов.
Бор, марганец, медь, цинк и другие микроэлементы по их количеству в земной коре принадлежат к распространенным элементам. Но содержание этих элементов неодинаково в различных почвах страны.
Исследования показали, что растения усваивают из почвы только те микроэлементы, которые переходят в почвенный раствор. Однако не все почвы содержат достаточное количество растворимых форм микроэлементов. Недостаток в микроэлементах восполняется в настоящее время введением в почву микроудобрений, содержащих бор, магний, марганец, цинк и др.
В связи с тем что эффективность микроудобрений в значительной мере зависит от свойств почв, остановимся кратко на их характеристике.
Подзолистые почвы бесструктурны, содержат мало перегноя и питательных веществ для растений.
Дерновые почвы по сравнению с подзолистыми более богаты перегноем и отличаются высоким плодородием.
Дерново-подзолистые почвы образовались под влиянием луговой и лесной растительности. Они характерны для лесо-степных районов; по составу и структуре занимают промежуточное положение между дерновыми и подзолистыми почвами. Содержание в них питательных веществ и перегноя колеблется в зависимости от принадлежности к геохимической провинции.
Торфяные почвы подразделяют на низинные и верховые торфяники. Низинные торфяники образовались из тростника, осок и другой подобной растительности. Этот торф богат азотом, но плохо доступен растениям. На этих торфяниках высокие урожаи сельскохозяйственных культур удается получать при внесении фосфорных и калийных удобрений. Верховые торфяники образовались из мхов. Они беднее азотом, чем низинные торфяники.
Черноземные почвы образовались под степной травянистой растительностью и залегают в зоне лесостепи и степи. Своим названием обязаны черному цвету верхнего слоя, богатого органическим веществом. Это наиболее плодородные почвы не только в нашей стране, но и во всем мире.
Каштановые почвы распространены в полупустынях. Имеют признаки солошхеватости. По своему плодородию приближаются к черноземам.
Сероземы. В этих почвах, расположенных на юго-востоке страны, содержание органического вещества иногда даже ниже, чем в до])ново-подзолистых почвах. Тем не менее при орошении эти почвы обеспечивают получение высоких урожаев многих ценных культур и особенно хлопчатника.
Перечисленные выше почвы содержат также неодинаковое количество микроэлементов.
Бор ученые считают одним из первых среди изученных микроэлементов и важным по своему значению в минеральном питании растений. Он играет особую роль в биохимических процессах, протекающих в растительных организмах. Одно из соединений бора — бура Na2B407 — было известно еще древним алхимикам и применялось ими более 1000 лет назад. Название «бор» происходит от арабского слова «борак», которым в то время называли белые кристаллические соли, в том числе и буру. Первооткрывателем элементарного бора считают французских ученых Жозефа Гей-Люссака и Луи Тенера, которые в 1808 г. при нагревании борной кислоты получили оксид бора В2О3, а затем восстановили его металлическим калием до бора.
В настоящее время бор известен в двух аллотропических модификациях (разновидностях) — аморфной и кристаллической. Интересно отметить, что аморфный бор в виде порошка бурого цвета получают путем восстановления оксида бора В203 магнием или натрием:
В208 + 3Mg - 2В + 3MgO + Q
Кристаллический бор получают путем кристаллизации его из расплавленного алюминия. Такой бор содержит небольшое количество алюминия и обладает твердостью, почти равной твердости алмаза.
В концентрированных щелочах бор растворяется с выделением водорода:
2В + 2К0Н + 2Н20 - 2КВОа + ЗН2
а концентрированные азотная и серная кислоты окисляют этот элемент в борную кислоту:
В + ЗНШз - Н3ВО3 + 3N02
Хотя бор и принадлежит к числу рассеянных элементов, однако содержание его в земной коре составляет 1,4 • 10~3% по массе, что ставит его в один ряд с наиболее распространенными элементами. Бор практически содержится во всех почвах, в воде морей, рек и озер. Высокое содержание бора находится в водах грязевых вулканов и нефтяных водах, а также в некоторых горячих источниках.
В нашей стране значительные месторождения борных руд с высоким содержанием бора имеются в Казахской ССР (Индерский район), на Кавказе в районе Пятигорска (залежи датолита CaHBSiOs, содержащего 6% бора). В небольших количествах бор встречается в сопочных грязях Таманского и Керченского полуостровов.
Бор в природе находится в основном в виде кислородных соединений, к которым относятся борная кислота (минерал сассолин) Н3В03, а также бура (тинкал) Na2B407 • 10Н2О, ашарит 2MgO * В203 • Н20 и колеманит 2СаО . ЗВ203 • 5Н20.
Борная кислота (а точнее, ортоборная) — это бесцветные кристаллы, малорастворимые в воде. При нагревании до 140 °С она теряет воду и переходит вначале в метаборную кислоту НВ02, а затем в тетраборную кислоту Н2В407 и, наконец, в оксид В203. При растворении в воде НВ02 и Н2В407, так же как и В203, переходят в Н3В03. Бура Na2B4C>7 образуется при действии щелочи на Н3В03:
2NaOH + 4И3ВО3 Na2B А + 7Н20
бура
Из раствора бура выделяется в виде больших бесцветных кристаллов Na2B407 • ЮН20. Растворимость их тоже мала. Число почвенных соединений бора, растворимых в воде, возрастает с севера на юг. Наиболее богаты бором почвы южных областей СССР, образовавшихся на древних морских глинах и других осадочных породах. К этим почвам относятся засоленные почвы, а также сероземы и каштановые.
Дерново-подзолистые почвы, красноземы и некоторые торфяные, занимающие примерно половину всей терри-
|
Название почвы |
Содержание бора, мг/кг сухой почвы |
|
|
общее |
растворенного в воде |
|
|
Сеооземы ....................................... |
20,0—80,0 |
0,7-0,5 |
|
Каштановые................................. |
5,0—15,0 |
0,5-1,5 |
|
Черноземы..................................... |
4,0—12 |
0,4-1,7 |
|
Топфяные ...................... |
i,0— i 0,0 |
0,05—2,5 |
|
Дерново-подзолпстые . |
J ,5-()6 |
0,1-0,5 |
|
Серые лесные .... |
1,5-9,0 |
0,3-0,7 |
тории страны, содержат меньше бора (табл. 2). Если мы попытаемся сравнить различные торфяные почвы по содержанию в них бора, то увидим, что количество бора колеблется в широких пределах от 0,05 до 2,5 мг/кг сухой почвы. Особенно бедны бором торфяники. Количество бора в торфяных почвах зависит также от степени их разложения. Чем .выше степень разложения торфа, тем больше бора находится в воднорастворимой форме.
Исследования показали, что для растений важно не столько общее содержание бора в почвах, сколько его количество в виде соединений, которые способны растворяться в воде. К ним относятся кальциевые и магниевые борные минералы: гидробороцит СаО • MgO • ЗВ203- 6Н20, ашарит 2MgO • В203 • Н20, которые хорошо растворяются в воде и поэтому довольно легко усваиваются растениями. Борная кислота в почве может образовывать комплексные соединения с гидроксидом алюминия А1(ОН)3 и железа Fe(OH)3, что приводит к переходу части бора в менее доступные для растений формы.
Бор может содержаться в различных соединениях, но степень доступности этих веществ далеко не одинакова для растений. Содержание растворимого в воде бора в почвах нашей страны приведено в таблице 3.
Содержание бора обязательно учитывается в сельском хозяйстве при применении микроудобрений. В практических и научных целях необходимо иметь карту содержания боря в почвах. Такая схематическая карта валового содержания бора в почвах европейской части СССР составлена советскими учеными. На этой карте выделены
|
Почвы |
Содержание бора, мг/кг почвы |
|
Дерново-подзолистые .... |
0,08—0,38 |
|
Черноземные.................................................. |
0,38—1,58 |
|
Сероземы ........................................................ |
0,23—0,62 |
|
Каштановые....................................... . . |
0,30—0,90 |
три основные почвенные области по содержанию бора. Первая область — это северная, включающая в основном зону тундры, таежную зону и содержащая наименьшее количество бора — до 24 мг/кг почвы. Вторая — средняя область — это зона лиственных лесов и лесостепная зона с содержанием бора 24—40 мг/кг почвы. И наконец, третья — южная область — это степная, пустынно-степная и горная зоны европейской части СССР с количеством бора от 40 до 100 мг/кг почвы.
В почвах нашей страны увеличение концентрации бора возрастает к востоку и югу европейской части.
Марганец. Минерал пиролюзит, содержащий марганец, был известен человечеству еще в глубокой древности. Но годом открытия элемента марганца считают 1774 г., когда его выделили в свободном состоянии.
Исходным веществом для получения многих соединений марганца служит природный пиролюзит. Если нагреть его в токе водорода до 300 °С, то можно получить зеленый порошок оксида марганца МпОг- При окислении марганца можно получить целый ряд оксидов: МпО, МпСЬ, МпОз, Мп207. Из них для сельского хозяйства наиболее интересен Мп02. Нерастворимый в воде оксид марганца Мп02 хорошо растворяется в кислотах с образованием солей:
MnOa'+;2HN(V=rMn (N03y+ NO +rH20,
Mn02 + 4HC1 - MnCl2 + Cl2 + 2HA 2Mn03 +'2H2S0/-r2Mn8043+ Oa*+[2HaO'
Эти соли марганца также растворимы в воде. Из насыщенных растворов соли марганца выделяются в виде
разовых: кристаллогидратов:. Mn€l| • 4H$0;-"MnS04 • 4HiO йли-Мп804•■БНзО,/.
Марганец относится к наиболее распространенным элементам в природе. Содержание его в земной коре составляет ~0,09%- Однако в земной коре он распределен неравномерно. Больше всего марганца сосредоточено на поверхности земли в виде малорастворимых соединений. В глубоких слоях земли марганца значительно меньше. Здесь он находится преимущественно в виде соединений, отличающихся хорошей растворимостью.
Наша страна располагает очень большими запасами марганцовых руд с высоким содержанием марганца. Широко известно Чиатурское месторождение пиролюзита на Кавказе, а также Никопольское па Украине. Немалыми запасахми марганцовых руд располагают Урал, Западная Сибирь и другие места нашей страны. За рубежом значительные месторождения марганцовых руд имеются в Австралии, Южной Америке, Индии.
В небольших количествах марганец входит в состав широко распространенных горных пород, большое его скопление в природе наблюдается в виде кислородных соединений и прежде всего минерала пиролюзита, состоящего из оксида марганца Мп02, а также других минералов — гаусманита МП3О4, браунита М112О3, ромбического манганита МП2О3 • Н20, родохрозита — марганцового шпата МпС03, родонита — кремнистого марганца Mn0Si02 и др.
Из горных пород марганец извлекается водой ив виде растворимых соединений сотнями тысяч тонн в год уносится реками в моря и океаны. Тем не менее проведенные анализы морской воды показали невысокое содержание в ней марганца (10~“7 и 10“60/о). Более значительное его количество было обнаружено в иле глубин океана в виде осажденного бурого гидроксида марганца Мп (0Н)4, который образуется окислением растворимых соединений двухвалентного марганца.
Содержание марганца в основных типах почв изучено по всей территории Советского Союза. Общее среднее содержание его в почвах равнинной части страны составляет 1 мг/кг. Однако количество марганца в пахотном слое различных почв неодинаково. Наибольшее его количество наблюдается в серых лесных почвах (табл. 4).
Для повышения урожайности важно не общее количество марганца в почве, а наличие его растворимых, доступных растениям соединений (табл. 4).
|
Название почвы |
Содержание марганца, мг/кг сухой почвы |
|
|
общее |
растворенного в воде |
|
|
Дерново-подзолистые |
270—720 |
14,0—38,0 |
|
Серые лесные.................... |
1600 |
2,0-8,0 |
|
Черноземы...................... |
370--840 1 |
1,6—10,6 |
В почвах марганец присутствует в виде ионов Мп2+, Мп3+ и Мп4+. Наибольшей растворимостью и доступностью для растений обладают соединения двухвалентного марганца, наименьшей — трех-, четырехвалентного марганца. Поскольку соединения трехвалентного марганца являются не очень устойчивыми, то в почве обычно присутствуют ионы Мп2+ и Мп4+. В кислых почвах найдены наиболее подвижные двухвалентные формы соединений марганца, количество которых возрастает по мере протекания в почве восстановительных процессов. Это в значительной мере обусловлено применением кислых азотных удобрений (аммиачной селитры и сульфата аммония). В таких условиях происходит восстановление трех-и четырехвалентного марганца до растворимых и доступных растениям соединений двухвалентного марганца. Наоборот, в щелочных и нейтральных почвах при усилении окислительных процессов двухвалентные соединения марганца переходят в трудноусвояемую растениями форму гидроксида марганца Мп(ОН)2.
При дальнейшем окислении этот гидроксид переходит в почти нерастворимый оксид:
2Мп (ОН)а + 02. = 2Мп03 + 2НаО
Количество растворимых, хорошо усвояемых растениями соединений марганца в одной и той же почве может также изменяться в зависимости от ее влажности.
Весной и осенью, когда содержание влаги в почве высокое, наличие подвижных соединений марганца возрастает и растения хорошо усваивают соединения двухвалентного марганца,
К соединениям двухвалентного марганца относятся соли хороню растворимые в воде: М.п (N0,3)2 * 6Н20, MnS04-4H20, MnS04-5H20, MnCl2 и MnCl2-4H20, а также фосфорнокислые соединения марганца. Например, катион двухвалентного марганца образует с ортофосфорной кислотой одно-, двух- и трехзамещенные соли. Правда, не зсе они одинаково растворимы в воде. Если дигидрофосфат марганца Mn (H2PO,i)o * 2Н20 растворяется в воде, а гидрофосфат МлНРС>4 * ЗН20 слабо растворяется, то фосфат марганца Мпз(РО4)2 • 7Н20 является т р уд нор а створ и м о й солью. Исследования показали, что кислые почвы содержат значительные количества растворимых дигидрофосфатов марганца, в то время как труднорастворимые фосфаты марганца находятся главным образом в нейтральных и слабощелочных почвах.
С органическими кислотами (молочной, муравьиной, уксусной) катион марганца образует соли, растворимые в воде: Мп(С3Н503)2 • ЗН20, Мп(НС02)2 • 2Н20, Мп(С2Н302)2 • 4Н20. Органические кислоты в основном не могут связать почвенный марганец в нерастворимые соединения. Исключение составляет оксалат марганца М11С2О4, представляющий собой слаборастворимую соль. Но в почве практически нет условий, которые бы способствовали накоплению этих солей.
Следует отметить, что действие марганцовых удобрений на урожай сельскохозяйственных культур очень сильно зависит от кислотности почв (показателя pH).
При каких же pH почвы необходимо вносить марганцовые удобрения? Оказывается, потребность растений в марганцовых удобрениях наблюдается при pH 5,8 и выше. Если pH почвенной среды становится ниже 5,8, то потребность растений в соединениях марганца, как правило, обеспечивается самой почвой.
Вот почему действие марганцовых удобрений, как было установлено многочисленными опытами, в большей степени проявляется на нейтральных и слабощелочных почвах, а также на почвах со слабокислой реакцией.
Медь. Этот элемент принадлежит к металлам, полезные свойства которого были издавна использованы человеком для своих нужд. Произошло это, видимо, потому, что медь чаще, чем другие металлы, можно встретить в самородках значительной величины, мимо которых не мог пройти даже первобытный человек.
Небольшие количества меди содержатся практически во всех почвах, в водах рек, морей и океанов. В природе медь встречается в основном в виде различных соединений, однако можно увидеть и самородок этого элемента. Распространенность меди в земной коре оценивается по- разному, но все ее количественные оценки находятся в пределах 0,003—0,01 %. Более 150 минералов содержат медь. Из них наибольшее значение имеют медный колчедан CuFeS2, медный блеск Cu2S, красная медная руда Си20, малахит (Си0Н)2С03 и многие другие,
И еще одно примечательное обстоятельство — наиболее богаты медью щелочные породы, которые содержат 0,02%.
В нашей стране главные месторождения медных руд сосредоточены в Казахстане, на Урале, в Армении и Узбекистане.
Медь в почвах преимущественно двухвалентна. Важнейшими солями меди являются сульфат меди CuS04 или медный купорос CuS04 ° 5Н20, хлорид меди СиС12-2Н20, нитрат меди Cu(N03)2 • ЗН20. Эти соли хорошо растворяются в воде. Установлено, что если медь поглощается органическими веществами, то она труднее вымывается из почвы. Этим объясняется, в частности, накопление меди в верхнем горизонте почв. Однако соединения меди в большинстве случаев весьма плохо усваивают растения. При минерализации органических веществ часть меди освобождается из жестких оков, в которые она заключена.
Однако затем медь вновь может поглощаться органическими веществами почв. Вот почему торфяно-болотные почвы, содержащие большое количество органических веществ, очень бедны медью, а растения, выращиваемые на них, страдают от недостатка этого микроэлемента.
В почвах наряду с подвижными соединениями меди имеются также нерастворимые.
К ним относятся оксиды меди Cu20, СиО, гидроксиды СиОН, Си(ОН)2, карбонаты Си2С03 и др.
В результате микробиологических процессов в почве образуются органические кислоты (молочная, муравьиная, уксусная), с которыми медь дает растворимые соединения:
Си (С3Н503)2 • 2НаО,
Си (НСОа)а,
Хотя эти соединения меди и связаны с органическими кислотами, но вполне доступны для растения.
Определить содержание меди во всех почвенных зонах нашей страны —не простое дело. Но такую трудоемкую работу проделали наши ученые, и теперь мы располагаем интересными сведениями о содержании меди практически во всех почвах Советского Союза.
Общее содержание меди в почвах нашей страны неодинаково и колеблется в значительных пределах — от 1 до 140 мг на 1 кг почвы (табл. 5).
|
Таблица 5 Общее содержание меди в почвах (по данным В. А. Ковды)
|
Значительное количество меди содержится в черноземах. Наиболее бедны медью торфяные почвы. Это объясняется тем, что в таких почвах медь прочно фиксируется органическими веществами и переходит в недоступную форму для питания растений.
Растворимые в воде соединения меди сосредоточены в почвах в виде солей минеральных и органических кислот. Нитриты, хлориды и сульфаты меди, а также комплексные соединения меди с органическими кислотами хорошо растворимы в воде.
На подвижность меди влияет увеличение степени кислотности почвы. Например, в случае применения кислых форм минеральных удобрений или просто подкисления почвенного раствора наблюдается переход соединений меди в более растворимое состояние. Другим фактором, влияющим на увеличение подвижности меди, является также минерализация органических соединений почвы.
В практике сельского хозяйства важное значение имеет не только обогащение почвы подвижными соединениями меди, но и закрепление их в пахотном слое. В этих случаях применяют известкование почв.
Более 40 лет ученые занимаются изучением влияния меди на рост и развитие различных сельскохозяйственных культур. Выявлен целый ряд закономерностей влияния меди на урожай.
Наука, как известно, не стоит на месте. Не только каждый год и каждый месяц, но даже каждый день вносит свой весомый вклад в важное общенародное дело —* повышение урожайности сельскохозяйственных культур. В вопросе изучения обеспеченности различных почв усвояемыми формами соединений меди как важнейшего фактора урожайности сделано очень много. Академик Я. В. Пейве, например, применительно к почвам Латвийской ССР, предложил группировки почв по обеспеченности медью, представленные в таблице 6.
|
Таблица 6 Уровни обеспеченности различных почв медью, усвояемой растениями
|
||||||||||||||
Подобные группировки содержания меди в почвах разрабатываются сейчас для основных почвенных зон нашей страны.
Ученые составили карту общего содержания меди в почвах европейской части СССР. Здесь наблюдается общая тенденция увеличения концентрации меди с 6,0 мг/кг на северо-западе до 60—80 мг/кг почвы на юго-востоке. Специфичность действия меди, которая не может быть заменена (как мы уже отмечали) другими элементами, доказана целым рядом исследователей на многочисленном экспериментальном материале.
На торфяных почвах растения всегда испытывают недостаток меди. Однако и среди торфяно-болотистых почв встречаются почвы как с высоким, так и с низким содержанием меди. Большое количество меди встречается главным образом в заиленных торфах.
Верховые известковые, а также низменные и близкие к ним переходные торфяные почвы, имеющие нормальную или пониженную зольность, содержат очень мало меди. С помощью спектрального метода анализа, позволяющего определить в почвах медь в количествах менее 0,001 %, физико-химической лабораторией Академии наук СССР было установлено, что общее содержание меди в различных торфяных почвах колеблется от 0,3 • 10~3 до 5,9 * 10-3 %. Опираясь на эти данные, несложными расчетами было определено, что в пахотном слое верхового торфа количество меди составляет около 2 кг/га, а низинного — 11 кг/га. Известно, что сельскохозяйственными культурами с 1 га почвы выносится в среднем 30—60 г меди. Ясно, что общий запас меди в торфяных почвах не так уж мал. Так почему же наибольший эффект от применения медных удобрений достигается именно на этих почвах?
Растения используют из почвы только подвижные, растворимые в воде соединения меди. К сожалению, наличие хорошо усвояемых форм меди в почвах невелико и колеблется от 1,1 до 7,8 на 1 кг почвы (табл. 7).
|
Таблица 7 Содержание растворимых форм меди в почвах (по данным М. В. Каталымова)
|
Дерново-подзолистые почвы бедны подвижными соединениями меди. Черноземы по наличию хорошо усвояемых форм меди приближаются к дерново-подзолистым, больше всего таких соединений в серых лесных почвах.
Цинк. Знакомство европейцев с цинком относится к концу средних веков. В Китае этот металл был известен значительно раньше. Производство цинка как промышленного металла в Европе началось в XVIII в. Практическое применение цинка значительно расширилось в XIX в., после того” как в 1805 г. была открыта способность этого металла прокатываться в горячем состоянии. В 1832 г. из цинка начали изготовлять отливки, а в последующие годы этим металлом стали пользоваться для самых разнообразных целей.
Цинк относительно широко распространен в природе. Он встречается в почве, горных породах, в воде рек, морей и океанов, во всех растительных и животных организмах. В золе некоторых ракушек исследователями было найдено до 12% цинка. Среднее содержание цинка по массе в земной коре оценивается приблизительно в 0,02%. Основные породы, где был найден цинк,— это рудообразующие минералы, среди которых прежде всего надо отметить цинковую обманку (сфалерит) ZnS и цинковый шпат (смитсонит) Z11CO3, а также цинкит (красную цинковую руду) ZnO и гидроцинкит ZnC03 e 2Zn (ОН)2. Большинство цинковых минералов относится к полиметаллическим (содержащим несколько металлов) рудам: виллемит Zti2Si04, франклинит (Zn, F'e, Mn)0 • (Fe, Mn)203, тростит (Zn, Mn)Si04 галмей или каламин Zn2Si04 • H20. Содержание цинка в этих рудах незначительное. Запасы минералов цинка чаще всего залегают со свинцовыми и серебряными рудами.. Залежи подобных полиметаллических руд имеются в Казахстане, на Урале, Алтае, Северном Кавказе и в Сибири. Большие количества цинка сосредоточены в США и Южной Америке (Перу и Аргентине), Канаде, Австралии, Италии, Испании и других странах.
Исследователи в разное время проводили определения количества цинка в различных почвах нашей страны.
В 1944 г. биохимической лабораторией АН СССР были изучены главнейшие типы почв Советского Союза. В 1957 г. результаты этой работы обобщил академик А. П. Виноградов. Несколько позднее (в 1959 г.) видный советский почвовед В. А. Ковда опубликовал данные по содержанию цинка в почвообразующих породах [I] и почвах (табл. 8).
Далеко не одинаково содержание цинка находится в кладовых почвообразующих пород. В базальтах, например, наибольшее количество цинка; почти в 2 раза меньше этого металла! в траншах, Меньше всего -цинка ’-заключено .в'лессе,". '
|
Содержание цинка в почвообразующих породах и почвах (по данным В. А. Ковды)
|
Содержание цинка в почвообразующих породах во многом определяет размещение этого элемента в различных почвенных зонах страны. Высокое накопление цинка в красноземах связано с почвообразующими породами, состоящими из базальтов и андезитов. Богатство черноземных почв гумусом определяет высокое содержание в них цинка. Большое количество цинка в почвах тундры связано с его наличием в почвообразующих породах. Заметно меньшее количество цинка в дерново-подзолистых, серых лесных и сероземных почвах. На взаимосвязь содержания цинка в почвообразующих породах и почвах страны указывают близкие средние значения имеющегося в них цинка (соответственно 60 и 50—56 мг/кг). При этом среднее содержание цинка в почвах всей нашей земли составляет 50 мг/кг.
На примерах бора, марганца, меди мы видели, что для растений важно не общее количество того или иного микроэлемента в почвах, а его подвижное содержание, хорошо усваиваемое растениями. Цинк в этом случае не является исключением. Не надо, однако, думать, что, чем больше общего цинка содержится в почве, тем большее количество его подвижной формы присутствует в ней. Прямой зависимости в этом нет. Что же тогда определяет содержание подвижного цинка в почвах? Проведенные исследования показали, что основным условием при этом является кислотность.
Увеличение кислотности почвы приводит к возрастанию подвижности цинка, и, наоборот, уменьшение pH до 6,0— 6,5 — резкому ослаблению. При pH более 7,0 подвижность цинка опять возрастает, так как образуются цинкаты-соединения Na2Zn02, в которые цинк входит в состав аниона Zn02~2. Интересно, что при внесении в почву высоких доз фосфатов подвижность цинка резко уменьшается.
Исследования, проведенные академиком Я. В. Пейве в условиях нечерноземной полосы нашей страны, показали, что содержание подвижного цинка колеблется в среднем от 0,12 до 20 мг на 1 кг почвы. Наименьшее количество этого цинка находится в нейтральных почвах, наоборот, кислые дерново-подзолистые и торфяные характеризуются повышенным содержанием подвижного цинка, причем его содержание возрастает с уменьшением pH.
Применительно к почвенным зонам Латвийской ССР Я. В. Пейве нашел, что содержание общего цинка варьирует от 21,7 до 43,7 мг на 1 кг почвы, а подвижного — еще в более широких пределах — от 0,5 до 26 мг на 1 кг почвы.
Наиболее бедны подвижным обменным цинком дерново-карбонатные почвы (0,5 мг на 1 кг сухой почвы). На основе этих полученных экспериментальных данных академик Я. В. Пейве разделил все почвы Латвийской республики по содержанию в них цинка на пять групп.
Многочисленные исследования, проведенные в нашей стране, показывают, что в различных почвах содержится неодинаковое количество цинка. Больше всего хорошо усвояемого цинка находится в дерново-подзолистой, серой лесной, а также в некоторых других почвах нечерноземной зоны. Среднее количество подвижного цинка в них колеблется в пределах 0,12—20,0 мг/кг сухой почвы.
Значительно меньше обменного цинка, чем в дерново- подзолистых и лесных почвах, содержится в черноземах, сероземах, бурых и каштановых почвах. В черноземах, например, находится 0,1—0,25 мг/кг обменного цинка. Эти почвы по количеству обменного цинка, пожалуй, значительно ближе стоят к дерново-карбонатным.
В сероземах Средней Азии содержание подвижного цинка составляет 0,9—0,12 мг/кг. В бурых почвах — 0,03—0,2 мг/кг, а в каштановых подвижного цинка несколько больше 0}06~—ОД4 мг/кг.
Если рассматривать содержание цинка по горизонтам отдельных почв, то наиболее богатыми по содержанию обменного цинка окажутся верхние перегнойные слои. С глубиной количество обменного цинка уменьшается.
Молибден. Шведский ученый Карл Шееле в 1778 г. впервые получил молибденовую кислоту. Для этого он воздействовал азотной кислотой на молибденовый блеск. В осадке им был получен белый остаток, обладающий кислотными свойствами. Это и была молибденовая кислота. В это же время К. Шееле сделал правильный вывод о том, что сам минерал, из которого он получил молибденовую кислоту, является не чем иным, как сульфидом нового элемента.
Сульфид молибдена в дальнейшем стал основной сырьевой рудой для получения металлического молибдена.
Молибден, хотя и относится к числу широко распространенных элементов (с содержанием в земной коре ~ 10-3 %), однако он сильно рассеян и поэтому считается редким элементом. Молибден в небольших количествах (это является его отличительной особенностью) встречается в природе повсюду: в различных породах и почвах, водах рек, морей и океанов, растительных и животных организмах. Поэтому его обнаруживают в золе древесных и многих других растений. Особенно богаты молибденом клубеньки бобовых растений. В них заключено больше молибдена, чем в почвах, надземных органах и семенах растений.
Этот элемент встречается в виде природного соединения молибденита (сульфида молибдена, или, как его еще называют, молибденового блеска) MoS2, напоминающего по внешнему виду графит. Надо сказать, что молибден из-за блестящего вида вначале принимали за графит. Концентрация молибдена, найденного в природных соединениях, обычно не превышает 1—2%.
Кроме молибденового блеска, одинаковую с ним распространенность имеют молибдит Fe203 • ЗМо03 • 7,5 • Н20 и вульфенит РЬМо04, в меньшей степени — повеллит СаМо04. Всего в природе известно около 20 молибденовых минералов.
В нашей стране имеются природные месторождения молибдена. Встречается молибден и в виде сульфидных руд, являющихся хорошим источником получения молибдена. Наибольшее количество молибдена встречается в кислых породах, в основных изверженных породах его меньше. Необходимо отметить, что высокое содержание молибдена обнаружено в почвах, прилегающих к молибденовым месторождениям. Общее среднее количество молибдена в почвах страны составляет, по данным академика А. П. Виноградова, 2,6 мг/кг. Содержание молибдена в различных почвах неодинаково, что хорошо видно из данных таблицы 9.
|
Таблица 9 Содержание молибдена в почвах СССР (по данным В. А. Ковды)
|
Наибольшее количество молибдена содержится в черноземах. Примерно вдвое ниже молибдена встречается в серых лесных, подзолистых и красноземных почвах. Наименьшее содержание молибдена наблюдается в каштановых почвах и сероземах.
Надо иметь в виду, что молибден характеризуется сильно выраженной биологической аккумуляцией. Поэтому окультуренные почвы содержат больше этого элемента. Количество молибдена в почвах зависит и от ее механического состава. Больше молибдена сосредоточено в почвах тяжелых — глинистых и суглинистых, а наиболее бедны этим элементом почвы легкие — песчаные и супесчаные. Подвижность молибдена далеко не одинакова не только для различных почв страны, но и для одного и того же типа почв (табл. 10).
В целом содержание подвижного молибдена в почвах невелико. Но в почвах одного и того же типа количество молибдена изменяется весьма существенно. Например, дерново-подзолистые почвы по количеству подвижного молибдена могут отличаться между собой в 24 раза, а черноземные — почти в 17 раз. Подвижность молибдена в почвах и его хорошая усвояемость растениями зависит прежде всего от реакции среды. Щелочная реакция блгГ-
|
Содержание подвижного молибдена в почвах СССР (по данным акад. Я. В. Пейве)
|
гоприятно действует на подвижность молибдена; Наоборот, в кислой среде содержатся менее доступные для растений соединения молибдена.
Поэтому даже при достаточном общем содержании молибдена в почве многие растения часто не могут извлечь из нее то небольшое количество этого элемента, которое необходимо для их роста и развития. Например, нормальный рост клевера наблюдался при pH 6,9—7,9 без дополнительного введения в почву молибдена. При более высокой кислотности на той же почве для получения большого урожая клевера приходилось применять молибденовые удобрения.
Гидроксиды железа и алюминия, фосфаты и коллоиды почв также способны поглощать МоО|“ и переводить его в менее усвояемую форму.
На кислых почвах потребность растений в молибдене- начинает проявляться при pH ниже 5,2. В целях увеличения количества подвижного молибдена в почву обычно вносят известь. Это мероприятие почти полностью устраняет необходимость добавлять молибденовые удобрения. Фосфорные удобрения способствуют увеличению подвижности молибдена в почве. Но если количество марганца в кислых почвах увеличивается, то это в свою очередь способствует переходу молибдена в труднодоступное для растений состояние.
При употреблении минеральных удобрений надо иметь в виду, что применение кислых форм удобрений увеличивает кислотность почвы, ограничивает подвижность молибдена и делает его малодоступным для усвоения растениями.
Таким образом, знание кислотности почвы при применении молибденовых удобрений крайне необходимо.
Кобальт. Впервые кобальт был получен алхимиком Брандтом в 1735 г. В средние века не могли полностью отделить соединения серебра от кобальта, который загрязнял серебро, или, как тогда говорили, портил этот благородный металл. Не зная действительной причины загрязнения серебра, это объясняли наличием в нем сверхъестественного существа — кобольда. Отсюда и пошло название этих руд, а затем и самого металла кобальта.
Кобальт относится к числу малораспространенных в природе металлов, но его не считают редким элементом. Содержание кобальта в земной коре составляет 1,1— 4 • 10~3%, причем 9% от общего количества этого элемента в земной коре находится в рассеянном состоянии. Наиболее высокие концентрации кобальта (3,2—10~~2%) обнаружены в основных силикатных породах, наиболее низкие (4,0 • 10~4%) —в кислых породах (гранитах, гра- нодиоритах); содержание кобальта в основных (2,4 • 10”3%) и средних (1*10~3%) породах занимает промежуточное положение.
Кобальт можно найти во всех осадочных образованиях суши и моря, где его средняя концентрация составляет 1,0 • 10""3%• Высокие концентрации кобальта в различных породах еще не указывают на то, что именно в них можно найти наибольшее количество этого металла. Дело в том, что запасы кобальта определяются количественным соотношением наиболее распространенных горных пород. В настоящее время подсчитано, что к кислым породам относятся 60% всех пород, к основным — 30,75%, к осадочным — 5%, к средним --4% и ультраосновным— 0,25%. Свыше 70% кобальта находится в основных породах.
Самородки кобальта в природе чрезвычайно редки. Распространен этот элемент главным образом в виде химических соединений — минералов, как самостоятельных, так и входящих в состав других минералов. К последним относятся сульфидные минералы никеля и железа: петландит (FeNi)S, никелистый пирротин (FeS) и халькопирит (CuFeSg), в которых содержание кобальта не превышает 0,3%. Как самостоятельный минерал кобальт встречается в арсеиидах (C0AS2 — смальтин, СоАэз — скутерудит и др.), сульфидах (Co3S4 — линнеит, CoS2 — кобальт-пирит и др.), а также в виде кобальтового блеска CoAsS, кобальтового цвета Со3 • (АэО^г • 8Н20 и др.[II] Перечисленные минералы часто встречаются с рудами серебра и по цвету мало чем отличаются друг от друга.
Содержание кобальта в почвах зависит в основном от его количества в почвообразующих породах (табл. 11).
|
Таблица И Содержание кобальта в почвообразующих породах (по данным В. А. Ковды)
|
Больше всего кобальта содержится в базальтах, меньше— в глинах и покровных суглинках. Пески и супеси наиболее бедны кобальтом (табл. 11).
|
Таблица 12 Содержание кобальта в почвах (по данным В. А. Ковды)
|
Почвы, образовавшиеся на базальтах и глинах, гораздо богаче кобальтом по сравнению с почвами, возникшими на песках и супесях (табл. 12).
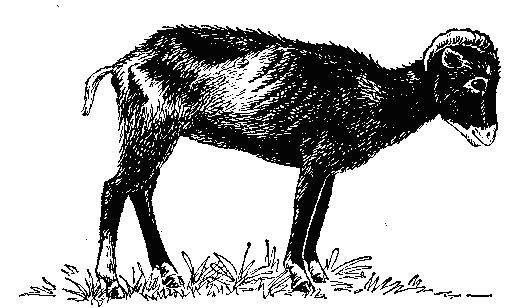
Рис. 1. Баран, больной акобальтозом (недостатком кобальта)
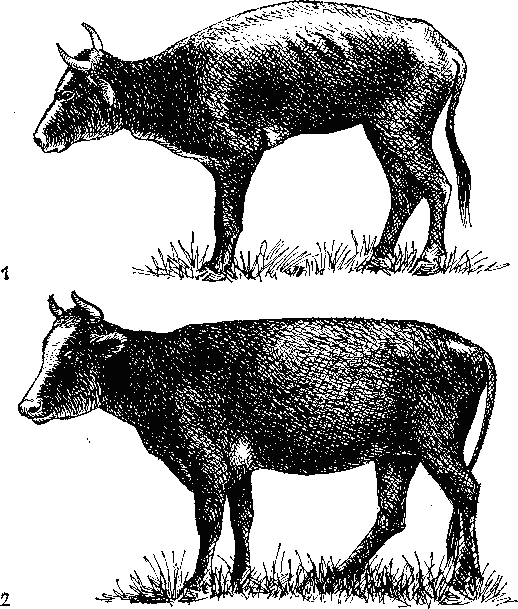
Рис. 2. Сухотка у рогатого скота (1), вызванная недостатком кобальта, здоровый рогатый скот (2) после подкормки кобальтом.
Наиболее богаты кобальтом каштановые и черноземные почвы, а наиболее бедны им дерново-подзолистые.
Для сельского хозяйства несомненный интерес представляют прежде всего черноземные, каштановые и дерново-подзолистые почвы. Среднее содержание кобальта в них колеблется от 3,1 до 8,6 мг/кг сухой почвы. Если в почвах кобальта содержится меньше 1,7—2,5 мг/кг, то такие почвы непременно должны быть обогащены этим элементом. Недостаток кобальта в почвах приводит к получению неполноценных кормов.
Если сельскохозяйственным животным давать такие корма, они заболевают акобальтозом и сухоткой (рис. 1, 2). Поэтому большое значение имеет наличие в почве подвижного кобальта. Здесь мы имеем несколько иную картину по распределению в почвах подвижного кобальта по сравнению с общим содержанием в почве этого элемента (табл. 13).
Т а б л и ц а 13
|
Содержание подвижного кобальта в почвах (по данным М. В. Каталымова)
|
Количество подвижного кобальта в почвах колеблется от 1,7 до 5,4 мг/кг. Наиболее богаты этим элементом серые лесные почвы.